Sự gia tăng của tình trạng đề kháng kháng sinh của vi khuẩn khiến các lựa chọn sử dụng kháng sinh trở nên hạn chế. Nhiều nghiên cứu đã được thực hiện nhằm tìm ra những yếu tố liên quan đến tình trạng gia tăng đề kháng kháng sinh, từ đó đưa ra các giải pháp khắc phục. Biofilm là một yếu tố quan trọng được tìm hiểu và có liên quan chặt chẽ với tình trạng đề kháng kháng sinh tại cơ sở y tế và cần lưu ý trong thực hành lâm sàng.
1. Đặc điểm tạo biofilm của vi khuẩn
Biofilm vi khuẩn hay màng sinh học vi khuẩn được định nghĩa là một cộng đồng vi khuẩn có khả năng sống và sinh sản như một quần thể, có cấu trúc và tương tác phức tạp, được bao quanh bởi lớp màng polymer ngoại bào.1, 2 Điều kiện để vi khuẩn hình thành biofilm là một bề mặt ổn định, cung cấp môi trường lý tưởng đủ độ ẩm và chất dinh dưỡng để vi khuẩn lưu trú và phát triển. Do đó, bề mặt của các thiết bị y tế xâm lấn trong cơ thể là một trong những vị trí thường xuất hiện biofilm nhất. Bên cạnh đó, vi khuẩn còn có thể bám vào bề mặt của nhiều mô trong cơ thể như da, mô liên kết, lớp nội mô mạch máu, khoang miệng, đường thở, mô xương…, từ đó gây tình trạng nhiễm trùng khó điều trị.1
Thành phần quan trọng của biofilm là chất nền polymer ngoại bào (Extracellular polymeric substances – EPS), được hình thành bởi các chất polysaccharid ngoại bào, ADN ngoại sinh, protein và lipid tiết ra bởi vi khuẩn trong các điều kiện môi trường khắc nghiệt. Mỗi thành phần của chất nền EPS đóng vai trò riêng. Các chuỗi polysaccharid đan vào nhau và liên kết thành mạng lưới dày đặc giúp hình thành cấu trúc của biofilm và ổn định chất nền. Protein (bao gồm cả enzym) duy trì sự ổn định của chất nền và khả năng bám dính vào bề mặt; các ADN ngoại sinh cũng củng cố sự hình thành biofilm, bảo vệ tính toàn vẹn của biofilm. Hơn 90% cấu trúc của biofilm là nước.1, 2
Thành phần và đặc tính của lớp EPS tạo ra bởi vi khuẩn gram dương và gram âm có sự khác biệt. Thành phần polysaccharid trong lớp EPS tạo ra từ vi khuẩn gram âm có thể trung tính hoặc tích điện âm, trong khi ở vi khuẩn gram dương thì tích điện dương.2
Đa số các chủng vi khuẩn trong tự nhiên có khả năng tạo biofilm.3 Đối với các vi khuẩn gây bệnh trên người, các vi khuẩn sinh biofilm phổ biến nhất là Pseudomonas aeruginosa, Staphylococcus epidermidis, Escherichia coli, Klebsiella pneumoniae, Proteus mirabilis, Streptococcus viridans, Staphylococcus aureus, và Enterococcus faecalis. Trong đó, các vi khuẩn thuộc họ Staphylocci gây ra 80% các trường hợp nhiễm khuẩn do thiết bị cấy ghép ở người. 2
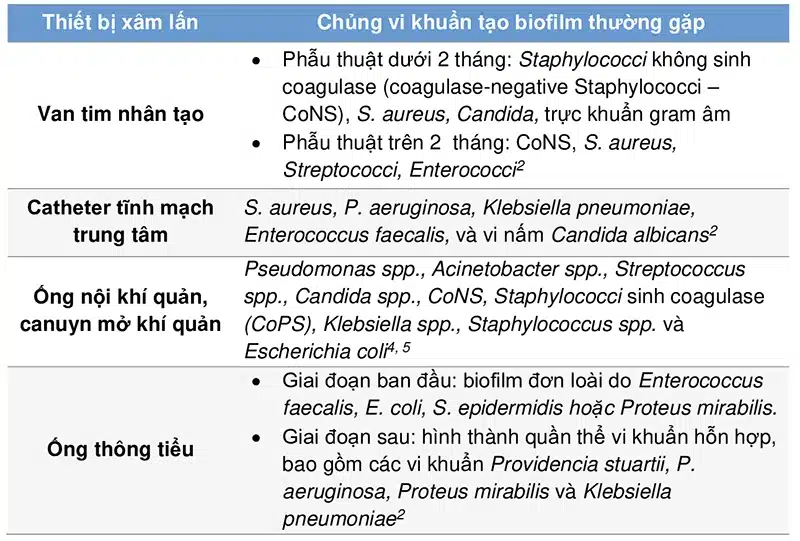
Tùy vào đặc điểm và vị trí của thiết bị xâm lấn, các vi khuẩn thường tạo biofilm gặp phải có thể khác nhau. Một số chủng vi khuẩn tạo biofilm thường gặp ở các loại thiết bị xâm lấn/cấy ghép được trình bày ở bảng 1.2, 4, 5
Bảng 1. Một số chủng vi khuẩn tạo biofilm thường gặp ở các thiết bị xâm lấn2, 4, 5
2. Quá trình hình thành biofilm của vi khuẩn
Quá trình hình thành biofilm của vi khuẩn gram âm và gram dương khá tương đồng, đều trải qua năm giai đoạn, bao gồm việc bám dính lên bề mặt vật chất, gắn kết vi khuẩn và sản sinh chất nền EPS, quá trình trưởng thành của biofilm thông qua hình thành các quần thể vi khuẩn, và phát tán vi khuẩn ra môi trường để bắt đầu hình thành biofilm mới (hình 1).1-3, 6
Ở bước đầu tiên, các vi khuẩn tự do di chuyển trong dịch cơ thể tiếp cận và bám dính lên các bề mặt thông qua các roi và lông mao. Quá trình này phụ thuộc vào các đặc điểm lý hóa của bề mặt, bao gồm độ nhẵn của bề mặt, mức độ ưa nước, điện tích bề mặt và khả năng tạo film. Vi khuẩn bám dính thông qua các lực vật lý như lực van der Waals hay lực tĩnh điện, do đó sự bám dính này tương đối lỏng lẻo và có thể bị phá vỡ.1
Ở giai đoạn tiếp theo, vi khuẩn bắt đầu tiết ra chất nền polymer ngoại bào,và sử dụng các thành phần trên bề mặt tế bào vi khuẩn để nhận diện và bám dính vào nhau thông qua các liên kết hóa học như tính kỵ nước, liên kết hydro, liên kết hóa trị, liên kết ion. Các bào quan lông, roi gắn các phần tử đặc hiệu cho các thụ thể (receptor-specific ligands) cũng tham gia vào quá trình hình thành sự kết dính giữa các vi khuẩn, giúp hình thành sự bám dính vĩnh viễn (không đảo ngược) với nhau và với bề mặt.1, 2
Tiếp theo, các tế bào vi khuẩn nhân lên và phân chia để hình thành các các vi quần thể. EPS ảnh hưởng tới quá trình hình thành các cấu trúc bên trong biofilm, nhận diện giữa các tế bào, truyền tín hiệu, thu nhận chất dinh dưỡng,… Nhờ đó, các vi quần thể trong biofilm có thể hợp tác với nhau về trao đổi cơ chất, vận chuyển chất chuyển hóa và loại bỏ chất thải. Trong nhiều trường hợp, trong một biofilm có thể chứa nhiều chủng vi khuẩn có quan hệ tương hỗ với nhau.1, 2
Giai đoạn trưởng thành của biofilm được khởi động khi có các yếu tố tín hiệu gắn vào tế bào vi khuẩn, gây ra sự thay đổi về biểu hiện gen của các tế bào. Sản phẩm của quá trình biểu hiện gen tạo ra các vật chất tích lũy cho lớp EPS làm ổn định cấu trúc biofilm, tạo ra lớp bảo vệ vi khuẩn khỏi kháng sinh hoặc bạch cầu đa nhân. Vi khuẩn tiếp tục nhân lên và tích lũy tạo thành các vi quần thể dày khoảng 100 µm.1, 2
Biofilm khi phát triển đủ lớn có thể xảy ra tổn thương do sự thay đổi của môi trường, kháng sinh, enzym phân hủy chất nền cạn kiệt chất dinh dưỡng… dẫn đến sự giải phóng và phát tán tế bào vi khuẩn ra môi trường và các bề mặt khác và tạo biofilm ở vị trí mới. Quá trình giải phóng tế bào có thể diễn ra chủ động hoặc bị động do hiện tượng bong tróc biofilm.1, 2
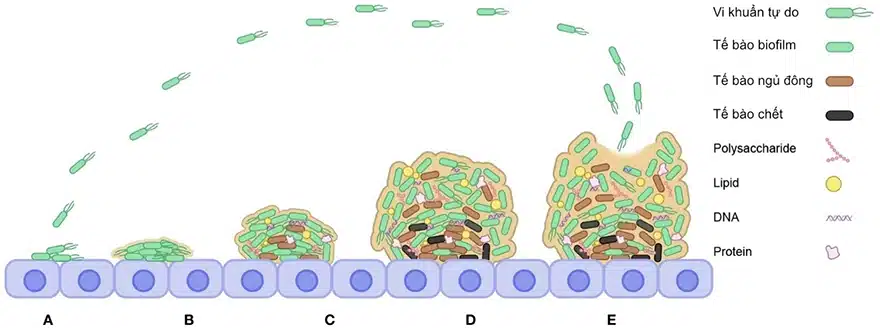
Hình 1. Vòng đời của biofilm.1 Các giai đoạn: (A) Bám dính tạm thời. (B) Bám dính vĩnh viễn. (C) Hình thành vi quần thể. (D) Trưởng thành. (E) Phát tán
3. Thách thức khi sử dụng kháng sinh trên vi khuẩn tạo biofilm
Với những đặc tính của biofilm, vi khuẩn tăng thêm khả năng dung nạp và kháng lại kháng sinh, gây ra khó khăn trong quá trình điều trị trên lâm sàng. Dưới đây là các cơ chế của biofilm nhằm chống lại tác dụng của kháng sinh tới vi khuẩn:
3.1. Thành phần lớp chất nền biofilm cản trở sự hấp thu kháng sinh vào bên trong biofilm
Các thành phần cấu tạo của lớp chất nền biofilm đều đóng vai trò bảo vệ vi khuẩn khỏi tác dụng của kháng sinh. Một số kháng sinh bị tạo phức hợp với các thành phần EPS, như kháng sinh nhóm aminoglycosid tích điện dương bị trung hòa bởi các ADN ngoại sinh tích điện âm. Lớp polysaccharid tạo hàng rào thấm chọn lọc, ngăn cản sự xâm nhâp của kháng sinh vào biofilm. Các enzym được bài tiết bởi vi khuẩn ra lớp chất nền có khả năng phân giải kháng sinh, làm giảm nồng độ kháng sinh tại biofilm (hình 2).6
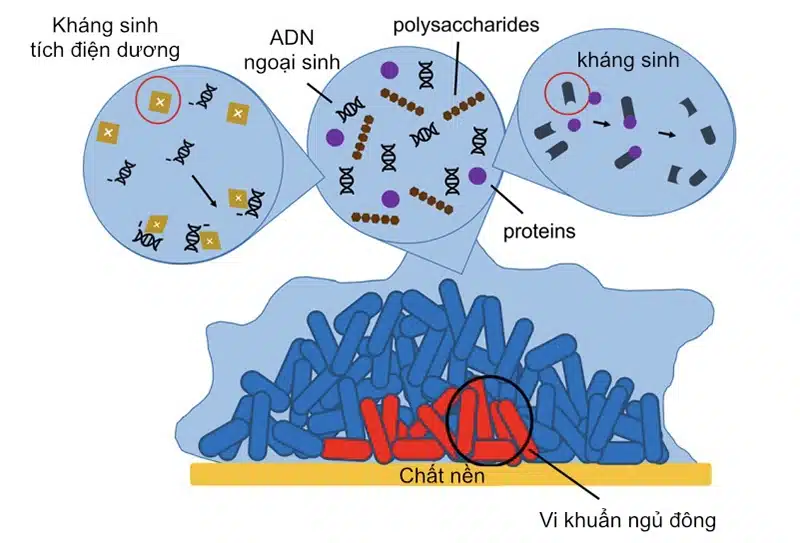
Hình 2. Cơ chế giảm tác dụng của kháng sinh nhờ lớp chất nền biofilm6
Nhờ các cơ chế nói trên, lớp chất nền của biofilm làm giảm nồng độ kháng sinh tại vị trí biofilm, dẫn đến nguy cơ nồng độ kháng sinh thấp hơn nồng độ ức chế vi khuẩn, tạo điều kiện chọn lọc các chủng vi khuẩn có đột biến kháng thuốc.6
3.2. Nồng độ lớn vi khuẩn trong biofilm tạo ra hiệu ứng inoculum
Số lượng vi khuẩn lớn tập trung trong biofilm tạo ra hiệu ứng inoculum: hiện tương kháng sinh giảm hiệu lực và độ nhạy cảm khi gặp nồng độ cao vi khuẩn. Các kháng sinh beta-lactam như ceftazidim, imipenem và kháng sinh tobramycin đã được chứng minh giảm nhạy cảm với biofilm của P.aeruginosa.6
3.3. Chuyển gen ngang (Horizontal Gene Transfer)
Các gen kháng thuốc có thể được trao đổi giữa các chủng vi khuẩn trong biofilm với nhau, giữa vi khuẩn không gây bệnh sang vi khuẩn gây bệnh, và giữa các vi khuẩn gây bệnh. Các vi khuẩn có thể trao đổi gen cho nhau qua 3 con đường (hình 3):
- Biến nạp: quá trình tiếp nhận ADN từ môi trường vào tế bào vi khuẩn
- Tải nạp: quá trình chèn ADN vào vi khuẩn bởi thực khuẩn thể
- Tiếp hợp, quá trình chuyển gen trên plasmid từ tế bào cho sang tế bào nhận thông qua tiếp xúc trực tiếp qua pili.6
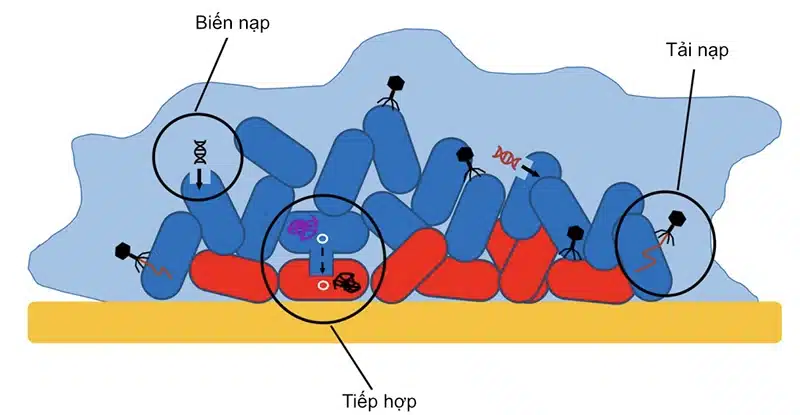
Hình 3. Ba con đường chuyển gen kháng thuốc giữa các vi khuẩn6
Các con đường nói trên được chứng minh xuất hiện phổ biến trong biofilm, từ đó làm tăng khả năng lan truyền các gen kháng thuốc được lựa chọn do vi khuẩn tiếp xúc với nồng độ kháng sinh dưới ngưỡng ức chế tối thiểu vi khuẩn. Gen blaNDM-1 mã hóa enzym carbapenemase và blaCTX-M mã hóa enzym ESBL là các ví dụ nổi bật của các gen kháng thuốc có thể được trao đổi giữa nhiều vi khuẩn gây bệnh gram âm.6
3.4. Các tế bào vi khuẩn ở trạng thái ngủ đông né tránh tác dụng của kháng sinh
Nhiều kháng sinh có cơ chế tác dụng dựa trên sự ức chế tổng hợp các thành phần quan trọng trong quá trình nhân lên của vi khuẩn. Trong biofilm, có nhiều tế bào vi khuẩn đang trong quá trình sinh trưởng ở các giai đoạn khác nhau. Bên cạnh, các vi khuẩn hoạt động mạnh thường ở bề mặt biofilm, còn những vi khuẩn thay đổi tốc độ chuyển hóa để trở thành dạng “ngủ đông” và thường tập trung sâu bên trong khối biofilm. Những vi khuẩn này tăng khả năng dung nạp kháng sinh, sống sót được khi tiếp xúc với kháng sinh ở nồng độ diệt khuẩn. Điều này có được do các vi khuẩn đó đã có sự biến đổi về kiểu hình, hạn chế tổng hợp các đại phân tử, kiềm chế quá trình sinh trưởng, và có thể tồn tại mà không cần những quá trình chuyển hóa vốn là đích tác dụng của kháng sinh.6
Nhờ có các vi khuẩn ngủ đông, biofilm có thể phục hồi số lượng vi khuẩn khi ngừng sử dụng kháng sinh, cho dù các tế bào vi khuẩn nhạy cảm đã bị tiêu diệt (hình 4).
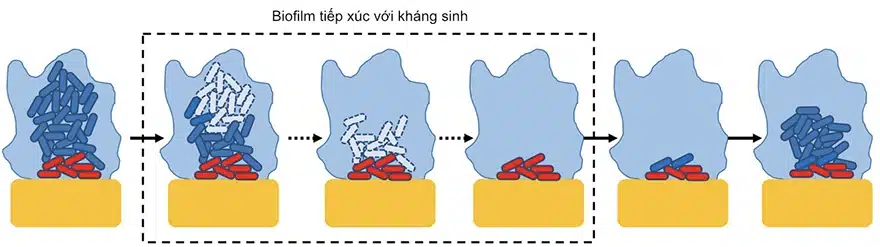
Hình 4. Biofilm phục hồi số lượng vi khuẩn sau khi tiếp xúc với kháng sinh6
3.5. Cảm biến số lượng (quorum sensing)
Cảm biến số lượng là quá trình điều hòa biểu hiện gen để đáp ứng với sự thay đổi về mật độ quần thể vi khuẩn trong biofilm. Cảm biến số lượng cho phép các tế bào trong biofilm phối hợp hành vi, thông qua các chất trung gian tín hiệu hóa học. Quá trình này có thể ảnh hưởng tới nhiều quá trình chuyển hóa của vi khuẩn, bao gồm cả quá trình tạo biofilm, và có thể làm tăng khả năng của vi khuẩn chống lại các tác nhân gây stress như chất oxy hóa, kim loại nặng, nhiệt độ, stress từ hệ thống miễn dịch của vật chủ và kháng sinh.6
4. Hoạt tính chống lại biofilm của kháng sinh
Với những đặc điểm của biofilm nhằm hạn chế tác dụng của kháng sinh vào vi khuẩn, chỉ có một số kháng sinh có khả năng chống lại tác dụng sinh biofilm. Đặc điểm quan trọng của kháng sinh có tác dụng chống lại biofilm bao gồm:
- Có khả năng xuyên qua lớp EPS và thấm vào bên trong biofilm mà không bị lớp chất nền EPS trung hòa hoặc phân hủy.
- Tác dụng lên đích cần thiết cho cả giai đoạn ngủ đông của vi khuẩn (VD: ARN polymerase) và thể hiện hoạt tính diệt khuẩn đối với các vi khuẩn ở dạng ngủ đông. 7-9
5. Một số kháng sinh có tác dụng chống biofilm vi khuẩn
Rifampicin
Rifampicin là kháng sinh điển hình và được nghiên cứu nhiều về tác dụng chống biofilm. Rifampicin có tác dụng diệt khuẩn dựa trên cơ chế ức chế ARN polymerase của vi khuẩn. Rifampicin vừa có khả năng thấm vào trong lớp chất nền EPS của biofilm vi khuẩn, vừa có khả năng diệt khuẩn mà không phụ thuộc vào tốc độ tăng tưởng của vi khuẩn, do đó có khả năng diệt khuẩn hiệu quả cả với những vi khuẩn đang ở trạng thái ngủ đông.10
Tác dụng chống biofilm của rifampicin được chứng minh rõ rệt nhất trên các chủng vi khuẩn Staphylocci trên nhiều nghiên cứu in vitro. Trên các chủng Streptococcus và Enterococcus, tác dụng chống biofilm của rifampicin yếu hơn.7, 8, 10 Tuy nhiên các nghiên cứu in vivo và trên người cho thấy kết quả không nhất quán.10 Do nhiều nghiên cứu chứng minh khả năng xuất hiện đề kháng, rifampicin luôn được khuyến cáo phối hợp kháng sinh trong điều trị.10
Nhiều hướng dẫn điều trị khuyến cáo phối hợp rifampicin với các kháng sinh chống lại Staphylococci (bao gồm cả MRSA) trong trường hợp bệnh nhân có nhiễm khuẩn liên quan tới các vật liệu nhân tạo có nguy cơ tạo ra biofilm như viêm khớp nhân tạo, viêm não thất, viêm màng não có đặt dẫn lưu dịch não tủy.11, 12 Liều dùng khuyến cáo của rifampicin trên trẻ nhũ nhi và trẻ em là 20 mg/kg/ngày (tối đa 600mg) chia 1 lần/ngày.11
Fluoroquinolon
Fluoroquinolon cũng là nhóm kháng sinh đã được chứng minh có tác dụng chống lại biofilm của vi khuẩn. Các kháng sinh fluoroquinolon là kháng sinh diệt khuẩn phổ rộng dựa trên cơ chế ức chế tổng hợp ADN gyrase của vi khuẩn gram dương và ADN topoisomerase IV của vi khuẩn gram âm. Tác dụng diệt khuẩn của fluoroquinolon không phụ thuộc vào tốc độ sinh trưởng của vi khuẩn, do đó có khả năng tác dụng tới biofilm.
Tác dụng chống biofilm của fluoroquinolon đã được chứng minh trên in vitro với các chủng vi khuẩn P.aeruginosa và E.coli.10, 13 Thêm vào đó, tác dụng chống biofilm cũng được chứng minh hiệu quả lâm sàng trong nhiễm khuẩn gram âm liên quan đến khớp giả. Hiệu quả chống biofilm của fluoroquinolon được tăng cường khi phối hợp cùng rifampicin.10
Hướng dẫn điều trị biofilm của Hiệp hội Vi sinh học lâm sàng châu Âu và các bệnh truyền nhiễm (ESCMID) khuyến cáo phối hợp fluoroquinolon trong điều trị các trường hợp nhiễm khuẩn liên quan tới thiết bị chỉnh hình nhân tạo.12
Fosfomycin
Fosfomycin là một kháng sinh phổ rộng, đã được chứng minh có tác dụng chống biofilm trên in vitro đối với nhiều loài vi khuẩn như Staphylococci, Enterococci hay E.coli sinh ESBL và P.aeruginosa.10, 14
Không chỉ có khả năng thấm vào biofilm và thể hiện tác dụng diệt khuẩn, các nghiên cứu còn cho thấy fosfomycin có khả năng ức chế quá trình tạo biofilm mới và gây phá vỡ cấu trúc của biofilm đã hình thành, từ đó tạo điều kiện cho các kháng sinh khác tăng khả năng thấm vào bên trong biofilm.10, 14 Phối hợp fosfomycin và rifampicin cho thấy hiệu quả tốt hơn trong việc ức chế tạo biofilm mới cũng như phá vỡ biofilm đã hình thành trước đó so với sử dụng fosfomycin hoặc rifampicin đơn độc.15
Nhờ tác dụng trên, fosfomycin có thể được phối hợp để làm tăng tác dụng in vitro của các kháng sinh khác trên các chủng vi khuẩn sinh biofilm ví dụ như aminoglycosid hay fluoroquinolon trên P.aeruginosa cũng như linezolid, minocyclin và vancomycin trên MRSA.10
Tetracyclin
Tetracyclin là nhóm kháng sinh kìm khuẩn phổ rộng với cơ chế ức chế tổng hợp protein thông qua ribosom 30S. Dù có tác dụng trên cả vi khuẩn gram âm và gram dương, tác dụng chống biofilm của tetracyclin chủ yếu được nghiên cứu trên vi khuẩn gram dương và bằng chứng còn khá hạn chế.9
Minocyclin và tigecyclin có tác dụng chống biofilm trên Staphylococcus spp., bao gồm S.aureus và S.epidermidis, cũng như Enterococci nhạy cảm hoặc kháng với vancomycin, khi phối hợp với các kháng sinh khác trong đó có rifampicin.9
Ái lực cao của các kháng sinh tetracyclin với chất nền khoáng chất của xương giúp cho kháng sinh đạt được nồng độ cao kể cả khi ngừng kháng sinh và là một ưu điểm của nhóm kháng sinh này khi chống lại biofilm. Tetracyclin có nhược điểm chỉ là kháng sinh kìm khuẩn.9
Daptomycin
Daptomycin tạo ra tác dụng diệt khuẩn nhờ cơ chế gắn vào màng tế bào vi khuẩn gây khử cực và mất điện thế màng, do đó có thể có tác dụng trên các vi khuẩn đang ở trạng thái tĩnh trong biofilm.9
Nghiên cứu in vitro cho thấy daptomycin thể hiện tác dụng diệt khuẩn và chống biofilm tương đương hoặc mạnh hơn so với rifampicin trên vi khuẩn S.epidermidis.16 Ngoài ra, một số nghiên cứu in vitro cho thấy daptomycin có thể là lựa chọn tiềm năng để phối hợp với rifampicin hoặc clarithromycin trong điều trị biofilm do S.aureus, hoặc phối hợp fosfomycin trong điều trị Enterococci kháng vancomycin.9
Glycopeptid
Các bằng chứng về tác dụng chống biofilm của vancomycin còn hạn chế và đều nghiên cứu trong phác đồ phối hợp với các kháng sinh có tác dụng chống biofilm khác. Tác dụng chống biofilm của vancomycin trên MRSA khi phối hợp với rifampicin chưa thống nhất giữa các nghiên cứu. Một số nghiên cứu cho thấy tác dụng hiệp đồng của vancomycin và fosfomycin trong việc chống biofilm trên S. aureus.9
Colistin
Nhiều nghiên cứu đã chứng minh tác dụng chống biofilm của colistin trên các chủng vi khuẩn gram âm, đặc biệt là biofilm do P.aeruginosa tạo ra. Một số nghiên cứu khác cho thấy tác dụng chống biofilm của colistin trên Enterobacterales. Tác dụng chống biofilm của colistin được cho là liên quan đến đích tác dụng trên lớp tế bào sâu hơn trong biofilm, ít hoạt động hơn. Colistin thể hiện tác dụng hiệp đồng cùng carbapenem chống lại cấu trúc biofilm của P.aeruginosa hoặc A.baumanii. 9
Tài liệu tham khảo
1. Zhao A, Sun J, Liu Y. Understanding bacterial biofilms: From definition to treatment strategies. Front Cell Infect Microbiol. 2023;13:1137947.
2. Sharma S, Mohler J, Mahajan SD, Schwartz SA, Bruggemann L, Aalinkeel R. Microbial Biofilm: A Review on Formation, Infection, Antibiotic Resistance, Control Measures, and Innovative Treatment. Microorganisms. 2023;11(6).
3. Sauer K, Stoodley P, Goeres DM, Hall-Stoodley L, Burmolle M, Stewart PS, et al. The biofilm life cycle: expanding the conceptual model of biofilm formation. Nat Rev Microbiol. 2022;20(10):608-20.
4. Deshmukh-Reeves E, Shaw M, Bilsby C, Gourlay CW. Biofilm Formation on Endotracheal and Tracheostomy Tubing: A Systematic Review and Meta-Analysis of Culture Data and Sampling Method. Microbiologyopen. 2025;14(4):e70032.
5. Mishra SK, Baidya S, Bhattarai A, Shrestha S, Homagain S, Rayamajhee B, et al. Bacteriology of endotracheal tube biofilms and antibiotic resistance: a systematic review. J Hosp Infect. 2024;147:146-57.
6. Liu HY, Prentice EL, Webber MA. Mechanisms of antimicrobial resistance in biofilms. NPJ Antimicrob Resist. 2024;2(1):27.
7. Albano M, Karau MJ, Greenwood-Quaintance KE, Osmon DR, Oravec CP, Berry DJ, et al. In Vitro Activity of Rifampin, Rifabutin, Rifapentine, and Rifaximin against Planktonic and Biofilm States of Staphylococci Isolated from Periprosthetic Joint Infection. Antimicrob Agents Chemother. 2019;63(11).
8. Zimmerli W, Sendi P. Role of Rifampin against Staphylococcal Biofilm Infections In Vitro, in Animal Models, and in Orthopedic-Device-Related Infections. Antimicrob Agents Chemother. 2019;63(2).
9. Ferreira L, Pos E, Nogueira DR, Ferreira FP, Sousa R, Abreu MA. Antibiotics with antibiofilm activity – rifampicin and beyond. Front Microbiol. 2024;15:1435720.
10. Ferreira L, Pos E, Nogueira DR, Ferreira FP, Sousa R, Abreu MA. Antibiotics with antibiofilm activity – rifampicin and beyond. Frontiers in Microbiology. 2024;15.
11. Tunkel AR, Hasbun R, Bhimraj A, Byers K, Kaplan SL, Scheld WM, et al. 2017 Infectious Diseases Society of America’s Clinical Practice Guidelines for Healthcare-Associated Ventriculitis and Meningitis*. Clinical Infectious Diseases. 2017;64(6):e34-e65.
12. Høiby N, Bjarnsholt T, Moser C, Bassi GL, Coenye T, Donelli G, et al. ESCMID∗ guideline for the diagnosis and treatment of biofilm infections 2014. Clinical Microbiology and Infection. 2015;21:S1-S25.
13. Tanaka G, Shigeta M, Komatsuzawa H, Sugai M, Suginaka H, Usui T. Effect of the growth rate of Pseudomonas aeruginosa biofilms on the susceptibility to antimicrobial agents: beta-lactams and fluoroquinolones. Chemotherapy. 1999;45(1):28-36.
14. Slade-Vitković M, Batarilo I, Bielen L, Maravić-Vlahoviček G, Bedenić B. In Vitro Antibiofilm Activity of Fosfomycin Alone and in Combination with Other Antibiotics against Multidrug-Resistant and Extensively Drug-Resistant Pseudomonas aeruginosa. Pharmaceuticals. 2024;17(6).
15. Liu Y, Ma W, Li M, Wu J, Sun L, Zhao W, et al. Antibacterial and antibiofilm activities of fosfomycin combined with rifampin against carbapenem-resistant Pseudomonas aeruginosa. Letters in Applied Microbiology. 2022;75(6):1559-68.
16. Leite B, Gomes F, Teixeira P, Souza C, Pizzolitto E, Oliveira R. In vitro Activity of Daptomycin, Linezolid and Rifampicin on Staphylococcus epidermidis Biofilms. Current Microbiology. 2011;63(3):313-7.
Biên tập: ThS.DS. Trần Nhật Minh, DS Lê Thị Nguyệt Minh






