Anthracyclines (doxorubicin, daunorubicin, epirubicin và idarubicin) là nhóm thuốc hóa trị được sử dụng rộng rãi trong điều trị nhiều loại ung thư. Nhưng việc sử dụng các hoạt chất này bị giới hạn bởi độc tính tim mạch (anthracycline-induced Cardiotoxicity – AIC) [1]. Đây là một biến chứng nguy hiểm, thường biểu hiện dưới dạng bệnh cơ tim và suy tim sung huyết không hồi phục, có khả năng gây tử vong [1,3].
Việc phát hiện sớm, phòng ngừa và quản lý AIC là cực kỳ quan trọng để tối ưu hóa kết quả điều trị ung thư mà không làm tổn hại nghiêm trọng đến chất lượng sống và tuổi thọ của bệnh nhân.
Theo thời gian khởi phát AIC được phân loại thành:
– Độc tính tim mạch cấp (Acute Cardiotoxicity): xảy ra trong hoặc ngay sau khi truyền một liều anthracycline duy nhất và tỷ lệ gặp dưới 1% bệnh nhân. Đặc điểm quan trọng của độc tính cấp tính là không phụ thuộc vào liều tích lũy của thuốc [2]. Các biểu hiện lâm sàng bao gồm: rối loạn chức năng thất, những thay đổi bất thường trên điện tâm đồ (ECG), rối loạn nhịp tim, hoặc hội chứng viêm cơ tim-màng tim [2]. Phần lớn các biểu hiện trên là thoáng qua và hồi phục trong vòng một tuầ
– Độc tính tim mạch mạn (Chronic Cardiotoxicity): là dạng phổ biến hơn, phụ thuộc liều tích lũy và gây ra giới hạn về liều trọn đời của anthracyclines [2]. Bao gồm:
+ Khởi phát sớm: Thường xuất hiện trong quá trình điều trị hoặc trong vòng một năm sau khi hoàn thành hóa trị.
+ Khởi phát muộn: Có thể xuất hiện nhiều năm sau khi kết thúc điều trị, đôi khi là sau 5 đến 10 năm, thường dẫn đến bệnh cơ tim hoặc suy tim sung huyết [2].
1. Cơ chế bệnh sinh
Độc tính tim mạch do anthracycline là một quá trình đa yếu tố, chủ yếu liên quan đến hai con đường phân tử riêng biệt nhưng có liên kết với nhau: Sự tương tác với Topoisomerase II β và Stress oxy hóa, đặc biệt là ở ty thể.
Topoisomerase II β (Topo II β): Con đường gây độc đích
Trong tế bào ung thư đang tăng sinh, các thuốc anthracyclines nhắm mục tiêu vào Topoisomerase II α để tiêu diệt tế bào khối u, nhưng cũng ảnh hưởng đến Topoisomerase II β (một isoform có nồng độ cao trong tế bào cơ tim trưởng thành) gây độc tim mạch [3,4]. Anthracyclines gắn vào phức hợp enzyme-DNA (nơi enzyme đã cắt sợi DNA) bằng liên kết cộng hóa trị [3,4]. Sự liên kết này ngăn chặn Topo II β hàn gắn lại các đoạn DNA bị cắt [4]. Điều này dẫn đến tổn thương DNA không thể hồi phục, đặc biệt tại các vùng genomic nhạy cảm, gây ra quá trình chết tế bào theo chương trình (apoptosis) của tế bào cơ tim [3].
Stress oxy hóa và tổn thương ty thể
Stress oxy hóa là sự mất cân bằng giữa các gốc oxy hóa tự do (ROS) và các chất chống oxy hóa nội sinh, đây được coi là cơ chế hàng đầu gây tổn thương tế bào cơ tim do anthracycline [5]. Anthracyclines kích thích NADPH oxidase (Nox) sản xuất superoxide theo hai cách:
+ Anthracyclines trực tiếp bị oxy hóa cấu trúc quinone của chúng thành gốc semiquinone, sau đó phản ứng với oxy để tạo ra các gốc oxy hóa tự do [5].
+ Anthracyclines cũng kích thích trực tiếp sự hoạt hóa của Nox, dẫn đến việc sản xuất các gốc oxy hóa tự do [5].
Superoxide kết hợp với NO tạo thành peroxynitrite, một chất oxy hóa cực mạnh, gây ra tổn thương tế bào cơ tim, giảm khả năng co bóp, thúc đẩy quá trình tự hủy tế bào của tế bào cơ tim [5].
Anthracyclines cũng làm ty thể trong tế bào cơ tim bị tổn thương nghiêm trọng do:
+ Liên kết cardiolipin: Anthracyclines có ái lực mạnh mẽ với cardiolipin, một thành phần quan trọng của màng trong ty thể. Sự liên kết này tạo ra phức hợp không thể đảo ngược, làm suy giảm chức năng cardiolipin và tăng sản xuất gốc superoxide [5].
+ Tổn thương DNA ty thể (mtDNA): Anthracyclines có khả năng chèn trực tiếp và nhanh chóng vào mtDNA, làm gián đoạn chuỗi vận chuyển điện tử, tạo ra các gốc oxy hóa tự do, suy giảm năng lượng tế bào (ATP) và dẫn đến quá trình tự hủy tế bào [5].
Ngoài ra, stress oxy hóa gây ra thoát các ion canxi làm gia tăng nồng độ canxi trong lưới nội bào cơ tim, từ đó kích hoạt các protease phụ thuộc canxi gọi là calpains [5]. Các calpains này làm thoái hóa titin, một thành phần cấu trúc chính của tế bào cơ tim, và kích hoạt caspase-12, dẫn đến quá trình chết tế bào theo chương trình và suy giảm chức năng co bóp, góp phần vào tăng độc tính cơ tim do anthracycline [5].
2. Ngưỡng liều tích lũy tối đa và chuyển đổi liều dùng giữa các Anthracyclines
Liều tích lũy tối đa khuyến nghị
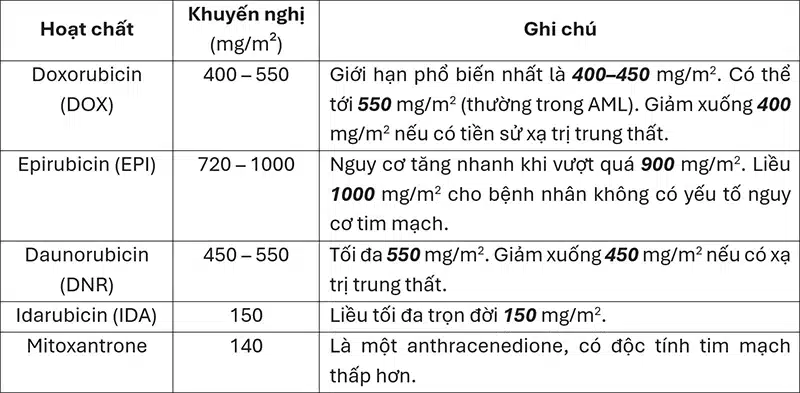
Sự khác biệt giữa các tổng liều tích lũy trọn đời (Maximum Cumulative Lifetime Dose – MCLD) phụ thuộc vào hoạt chất và bối cảnh lâm sàng [1,6].
Bảng 1. Liều tích lũy tối đa khuyến nghị của anthracyclines-anthracenediones
Tỷ lệ chuyển đổi liều (Dose Equivalence Ratios)
Trong trường hợp bệnh nhân nhận nhiều loại anthracyclines khác nhau trong suốt quá trình điều trị, cần phải quy đổi tổng liều tích lũy về liều tương đương doxorubicin để đánh giá tổng nguy cơ độc tính tim mạch. [7]
Bảng 2. Tỷ lệ tương đương liều so với doxorubicin (DOX = 1.0)
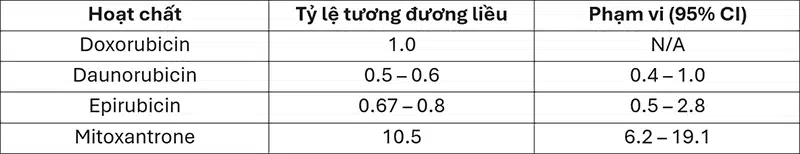
Tỷ lệ chuyển đổi này giúp các nhà lâm sàng có cái nhìn toàn diện hơn về tổng mức độ nhiễm độc tim mạch của bệnh nhân.
3. Chẩn đoán và theo dõi độc tính tim mạch
Chiến lược chẩn đoán và theo dõi hiện đại tập trung vào việc phát hiện rối loạn chức năng thất trái thông qua các thăm dò cận lâm sàng, trước khi có triệu chứng lâm sàng để có thể can thiệp sớm.
Theo các hướng dẫn của Hiệp hội Tim mạch Châu Âu (ESC) và Hiệp hội Ung thư Lâm sàng Hoa Kỳ (ASCO) độc tính tim mạch được xác định bằng sự suy giảm phân suất tống máu thất trái (LVEF) so với giá trị ban đầu: giảm >10% LVEF so với giá trị ban đầu và LVEF cuối cùng < 50% [8]. Các yếu tố tim mạch nghiêm trọng khác được xem xét trong tiêu chuẩn chẩn đoán bao gồm: suy tim, tử vong do tim, hội chứng mạch vành cấp và rối loạn nhịp tim đe dọa tính mạng [8]. Đánh giá LVEF bằng siêu âm tim qua thành ngực (TTE) vẫn là công cụ tiêu chuẩn để xác định độc tính tim mạch trên bệnh nhân ung thư. Việc sử dụng LVEF 3D-TTE được khuyến nghị để tăng độ chính xác trong đánh giá chức năng thất [9].
Global Longitudinal Strain (GLS) là một chỉ số siêu âm tim cho kết quả nhạy hơn LVEF trong việc phát hiện những thay đổi sớm nhất của cơ tim: giảm tương đối GLS >15% so với giá trị nền là ngưỡng chẩn đoán rối loạn chức năng tim [20].
Ngoài ra các dấu ấn sinh học tim mạch như Troponin tim (cTn) và Peptide lợi niệu Natri (Natriuretic Peptides – NP/BNP) đóng vai trò quan trọng trong việc theo dõi. Mức độ tăng của cTn và BNP có thể được áp dụng trong phân tầng mức độ nặng của bệnh tim mạch nền, giúp đánh giá tiên lượng, đặc biệt là ở những bệnh nhân tử vong sớm [9,21].
Hướng dẫn ESC 2022 khuyến nghị một lịch trình theo dõi cá nhân hóa dựa trên nguy cơ nền của bệnh nhân [9]:
– Đánh giá ban đầu: LVEF và GLS được khuyến nghị trước khi bắt đầu điều trị anthracycline đối với bệnh nhân nguy cơ cao và rất cao [9].
– Theo dõi trong quá trình điều trị:
+ Nguy cơ Cao/trung bình: Theo dõi cTn và NP/BNP được khuyến nghị cân nhắc mỗi hai chu kỳ trong quá trình hóa trị anthracycline [9].
+ TTE (tất cả nhóm nguy cơ): LVEF và GLS nên được cân nhắc thực hiện sau khi đạt liều tích lũy ≥ 250 mg/m2 doxorubicin tương đương [9].
– Theo dõi sau điều trị: Cần theo dõi các dấu ấn sinh học trong vòng 3 tháng sau khi điều trị [9]. Đối với những người sống sót sau ung thư có nguy cơ cao, TTE nên được xem xét tại các mốc năm thứ 1, 3, 5 sau điều trị và sau đó là 5 năm một lần [9].
4. Chiến lược phòng ngừa
Chiến lược phòng ngừa độc tính tim mạch của anthracycline bao gồm: thay đổi phương pháp sử dụng anthracycline, dự phòng bằng thuốc bảo vệ tim mạch, giám sát các yếu tố nguy cơ tim mạch.
Việc sử dụng anthracycline dạng liposome (ví dụ: Pegylated Liposomal Doxorubicin) đã được chứng minh là làm giảm đáng kể độc tính tim mạch so với dạng bào chế quy ước [1,10]. Truyền kéo dài anthracycline giúp nồng độ đỉnh trong huyết tương thấp hơn, từ đó giảm đáng kể tích lũy thuốc trong mô tim. Với nồng độ đỉnh thấp thuốc vẫn duy trì hiệu quả chống ung thư [10]. Tôn trọng và tuân thủ MCLD, cũng như tính toán chính xác liều tích lũy tương đương (DED) khi chuyển đổi hoạt chất, là biện pháp phòng tránh rủi ro cơ bản và quan trọng nhất [1].
Dexrazoxane là thuốc bảo vệ tim mạch duy nhất được FDA phê duyệt để sử dụng cùng anthracyclines [11]. Các nghiên cứu gần đây cho thấy cơ chế bảo vệ của thuốc là thông qua ức chế Topo II β ở tế bào cơ tim [11]. Dexrazoxane được khuyến cáo sử dụng cho bệnh nhân có nguy cơ cao, đặc biệt là khi liều tích lũy doxorubicin dự kiến vượt quá ngưỡng 250–300 mg/m2 [11]. Ngoài ra, các hướng dẫn hiện hành ủng hộ việc sử dụng các thuốc điều trị suy tim kinh điển, như thuốc ức chế men chuyển angiotensin (ACE-I) hoặc thuốc đối kháng thụ thể angiotensin (ARB) và/hoặc chẹn beta để phòng ngừa, điều trị độc tính trên tim mạch của anthracyclines [9].
5. Kết luận
Độc tính tim mạch do anthracycline (AIC) vẫn là một thách thức lớn trong điều trị ung thư và đòi hỏi phương pháp tiếp cận đa chuyên khoa dựa trên bằng chứng khoa học. Trên lâm sàng, cần tuân thủ nghiêm ngặt các giới hạn liều tích lũy tối đa trọn đời (MCLD) và sử dụng chính xác tỷ lệ chuyển đổi liều tương đương doxorubicin (DED) khi sử dụng nhiều hoạt chất. Ap dụng các chiến lược phòng ngừa như truyền kéo dài anthracycline, sử dụng các dạng bào chế mới, giám sát các yếu tố nguy cơ tim mạch bằng các kỹ thuật hình ảnh tiên tiến (LVEF và GLS) và các dấu ấn sinh học (cTn và NP/BNP) là giải pháp cần thiết để tối ưu hóa kết quả điều trị của bệnh nhân ung thư.
Tài liệu tham khảo (APA 7)
1. Bitar, O. M., Patel, K., Dassanayaka, S., & Shrestha, A. (2024). Anthracycline-Induced Cardiotoxicity. StatPearls Publishing. Truy cập từ: https://www.ncbi.nlm.nih.gov/books/NBK599501/; https://www.ncbi.nlm.nih.gov/books/NBK538187/
2. Hyman, G. A., & Hurria, A. (2020). Anthracycline-related cardiotoxicity in older patients with acute myeloid leukemia: Diagnosis, monitoring, and management. Blood Advances, 4(4), 762-772.
3. Ly, V., Leduc, C., & Jaxel, C. (2018). Human Top2α and Top2β are the cellular targets of anthracyclines. Molecules, 23(12), 3326.
4. Spallarossa et al., (2021). Anthracycline-Induced Cardiotoxicity: Molecular Mechanisms and Novel Therapeutic Approaches. Cells, 10(11), 3058.
5. Sun et al., (2023). Molecular details of anthracycline-induced cardiotoxicity oxidative stress. Frontiers in Cardiovascular Medicine, 10. Truy cập từ https://www.ncbi.nlm.nih.gov/books/NBK538187/
6. D’Silva et al., (2019). Dose equivalence ratios for anthracycline and anthracenedione-related cardiotoxicity. Journal of Clinical Oncology, 37(15), 1279-1286.
7. BC Cancer. (2023). Pharmacy FAQ: Lifetime Cumulative Doses. Truy cập từ http://www.bccancer.bc.ca/pharmacy-site/Documents/Pharmacy%20FAQs/Pharmacy-FAQ-Lifetime-Cumulative-Doses.pdf
8. Lancellotti et al., (2022). Global Longitudinal Strain as a Marker for Subclinical Cardiac Dysfunction in Cardio-Oncology. Cardio-Oncology, 8(1), 17.
9. Senthilnathan, V. M., & Prasad, V. B. (2024). Early prediction of anthracycline-induced cardiotoxicity using cardiac biomarkers and echocardiography. Indian Heart Journal, 76(2), 160-164.
10. Chen et al., (2023). Dexrazoxane Can Effectively Alleviate ARC. Pharmaceuticals, 17(12), 1739.
11. Liu et al., (2024). Safety evaluation of the combination with dexrazoxane and anthracyclines: A disproportionality analysis based on the Food and Drug Administration Adverse Event Reporting System database. Pharmaceuticals, 17(12), Article 1739. https://doi.org/10.3390/ph17121739
Biên tập: ThS.DS. Nguyễn Văn Dũng, DS. Nguyễn Việt Anh