Đặt vấn đề
Vắc xin 9vHPV được phê duyệt với mục đích phòng ngừa virus HPV typ 16, 18, 31, 33, 45, 52, và 58 (nguyên nhân dẫn đến hơn 90% trường hợp ung thư cổ tử cung, các loại ung thư liên quan HPV như âm đạo, âm hộ, hậu môn, hầu họng) và HPV typ 6,11 (nguyên nhân gây ra xấp xỉ 90% trường hợp mụn cóc sinh dục, u nhú đường hô hấp). Tổ chức Y tế Thế giới khuyến cáo nên theo dõi dài hạn khả năng sinh miễn dịch, hiệu quả, an toàn của vắc xin ngừa HPV.
Mục tiêu nghiên cứu
Đánh giá khả năng sinh miễn dịch, hiệu quả, độ an toàn của vắc xin 9vHPV ở trẻ nam và nữ vào tháng 126 (10 năm sau 3 liều vắc xin 9vHPV).
Phương pháp nghiên cứu
Thiết kế nghiên cứu: Nghiên cứu mô tả, tiến cứu, đa trung tâm
Đối tượng nghiên cứu: Trẻ nam và nữ 9-15 tuổi đã được tiêm 3 liều vắc xin 9vHPV (ngày 1, tháng 2, tháng 6) chấp nhận tham gia vào nghiên cứu theo dõi dài hạn.
Địa điểm nghiên cứu: Nghiên cứu dài hạn được tiến hành tại 40 địa điểm nghiên cứu, thuộc 13 quốc gia (Bỉ, Brazil, Colombia, Costa Rica, Peru, ba Lan, Nam Phi, Hàn Quốc, Tây Ban Nha, Thụy điển, Đài Loan, Thái Lan và Mỹ).
Tiêu chí chính: đánh giá phản ứng sinh kháng thể kháng HPV 6, 11, 16, 18, 31, 33, 45, 52 và 58 trong 10 năm sau liều vắc xin thứ 3 bằng xét nghiệm miễn dịch Luminex.
Tiêu chí phụ: đánh giá hiệu quả lâu dài của vắc xin dựa trên tỷ lệ mắc nhiễm trùng dai dẳng (thời gian ≥ 6 tháng ± 1 tháng cửa sổ thăm khám) và bệnh tật liên quan đến HPV 6/11/16/18/31/33/45/52/58.
Đánh giá độ an toàn của vắc xin bao gồm các báo cáo tử vong và biến cố bất lợi liên quan đến vắc xin.
Kết quả
Mẫu nghiên cứu: Trong số 2553 trẻ nam và nữ đã nhận 3 liều vắc xin, 1272 trẻ đồng ý tham gia vào nghiên cứu theo dõi dài hạn và 922 trẻ (72,5%) đã hoàn thành nghiên cứu.
Tiêu chí chính (tính sinh miễn dịch):
Kết quả: 99.6% đến 100% trẻ có đáp ứng miễn dịch vào tháng thứ 7 và 81.3% đến 97.7% duy trì đáp ứng miễn dịch vào tháng thứ 126, tùy thuộc vào chủng HPV.
Dựa vào xét nghiệm HPV-9 IgG-LIA có độ nhạy cao hơn, 94.9% đến 100% trẻ có đáp ứng miễn dịch vào tháng thứ 126.
Kết quả được thể hiện trong đồ thị dưới đây (Hình 1).
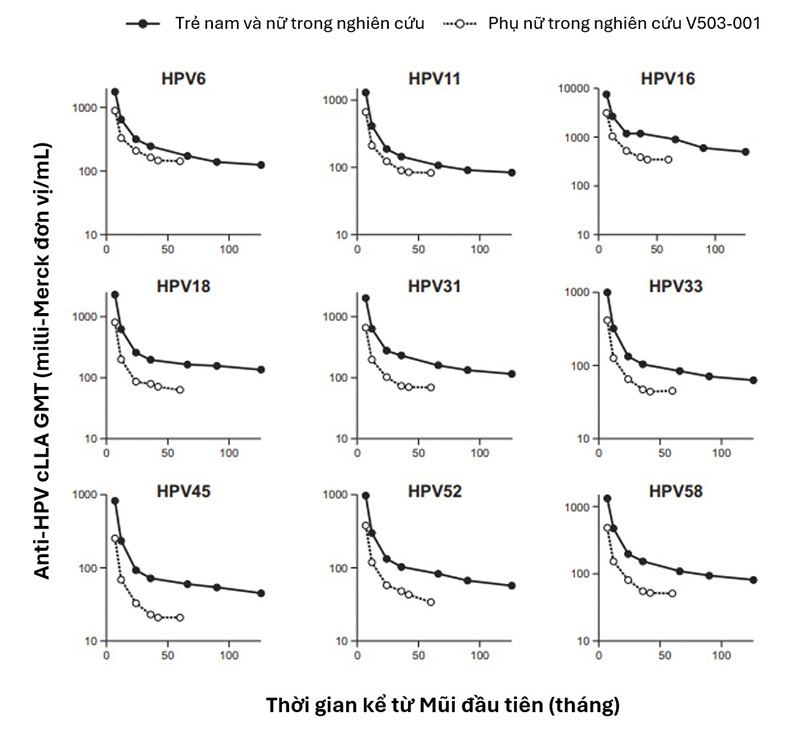
Hình 1: Kháng thể Anti-HPV cLIA GMTs sau 10 năm tiêm vắc xin ở trẻ nam và nữ từ 9 đến 15 tuổi và phụ nữ từ 16 đến 26 tuổi
Tiêu chí phụ (hiệu quả):
- Sau thời gian theo dõi, không có trường hợp nào mắc bệnh ung thư biểu mô cổ tử cung mức độ nặng hoặc ung thư âm đạo liên quan đến HPV typ 6/11/16/18/31/33/45/52/58. Có 1 trường hợp mắc ung thư cổ tử cung mức độ 1 và xét nghiệm PCR dương tính với HPV typ 16, 39, 59 vào tháng thứ 84 nhưng kết quả tế bào cổ tử cung âm tính ở những lần khám tiếp theo.
- Tỉ lệ mắc các bệnh và nhiễm trùng nằm ngưỡng dự kiến dựa trên các nghiên cứu trước đây về vắc xin 9vHPV.
- Tỉ lệ nhiễm trùng liên quan đến HPV35/39/51/56/59 trong vòng 6 tháng là 4/10000 người-năm với nữ và 261.5/ 10 000 người-năm với nam.
- Tỉ lệ mắc bệnh liên quan đến HPV35/39/51/56/59 ở trẻ nữ là 68.8/10.000 người-năm. Không có trường hợp nào mắc bệnh liên quan đến HPV35/39/51/56/59 ở trẻ nam.
- Kết quả chi tiết được thể hiện trong Bảng 2.
Bảng 2: Tỉ lệ mắc bệnh và nhiễm trùng liên quan đến HPV6/11/16/18/31/33/45/52/58 ở trẻ em tham gia theo dõi dài hạn
| Trẻ nữ (N=5971) | Trẻ nam (N=5301) | |||||
| Cases/n | Người- năm theo dõi |
Tỉ lệ/ 10 000 |
Cases/n | Người- năm theo dõi |
Tỉ lệ/ 10 000 |
|
| Bệnh tật hoặc nhiễm trùng liên quan đến HPV6/11/16/
18/31/33/45/52/58 trong vòng 6 tháng |
24/872 | 4579,6 | 52,4
(33,6-78,0) |
7/261 | 1282,7 | 54,6
(21,9-112,4) |
| Nhiễm trùng trong vòng 6 tháng liên quan đến HPV6/
11/16/18/31/33/45/52/58 |
24/872 | 4579,6 | 52,4
(33,6-78,0) |
7/261 | 1282,7 | 54,6
(21,9-112,4) |
| HPV6/11/16/18 | 22/870 | 4580,4 | 48,0
(30,1-72,7) |
1/261 | 1296,1 | 7,7
(0,2-43,0) |
| HPV6 | 4/847 | 4520,4 | 8,8
(2,4-22,7) |
0/255 | 1273,4 | 0,0
(0,0-29,0) |
| HPV11 | 0/847 | 4530,1 | 0,0
(0,0-8,1) |
1/255 | 1270,9 | 7,9
(0,2-43,8) |
| HPV16 | 17/860 | 4541,3 | 37,4
(21,8-59,9) |
0/260 | 1293,0 | 0,0
(0,0-28,5) |
| HPV18 | 1/867 | 4627,2 | 2,2
(0,1-12,0) |
0/259 | 1285,9 | 0,0
(0,0-28,7) |
| HPV31/33/45/52/58 | 2/872 | 4649,5 | 4,3
(0,5-15,5) |
6/261 | 1285,2 | 46,7
(17,1-101,6) |
| HPV31 | 0/855 | 4657,1 | 0,0
(0,0-8,1) |
2/259 | 1287,6 | 15,5
(1,9-56,1) |
| HPV33 | 1/866 | 4625,7 | 2,2
(0,1-12,0) |
0/259 | 1294,0 | 0,0
(0,0-28,5) |
| HPV45 | 0/871 | 4652,5 | 0,0
(0,0-7,9) |
1/261 | 1292,6 | 7,7
(0,2-43,1) |
| HPV52 | 0/870 | 4645,5 | 0,0
(0,0-7,9) |
4/261 | 1286,8 | 31,1
(8,5-79,6) |
| HPV58 | 1/863 | 4611,5 | 2,2
(0,1-12,1) |
0/259 | 1293,2 | 0,0
(0,0-28,5) |
| Nhiễm trùng trong 12 tháng liên quan đến HPV6/11/16/
18/31/33/45/52/58 |
9/872 | 4621,1 | 19,5
(8,9-37,0) |
2/261 | 1294,2 | 15,5
(1,9-55,8) |
| HPV6/11/16/18 | 8/870 | 4619,9 | 17,3
(7,5-34,1) |
0/261 | 1298,6 | 0,0
(0,0-28,4) |
| HPV6 | 2/847 | 4524,4 | 4,4
(0,5-16,0) |
0/255 | 1273,4 | 0,0
(0,0-29,0) |
| HPV11 | 0/847 | 4530,1 | 0,0
(0,0-8,1) |
0/255 | 1273,4 | 0,0
(0,0-29,0) |
| HPV16 | 5/860 | 4576,8 | 10,9
(3,5-25,5) |
0/260 | 1293,0 | 0,0
(0,0-28,5) |
| HPV18 | 1/867 | 4627,2 | 2,2
(0,1-12,0) |
0/259 | 1285,9 | 0,0
(0,0-28,7) |
|
HPV31/33/45/52/58 |
1/872 | 4651,4 | 2,1
(0,1-12,0) |
2/261 | 1294,2 | 15,5
(1,9-55,8) |
| HPV31 | 0/855 | 4567,1 | 0,0
(0,0-8,1) |
0/259 | 1289,2 | 0,0
(0,0-28,6) |
| HPV33 | 1/866 | 4625,7 | 2,2
(0,1-12,0) |
0/259 | 1294,0 | 0,0
(0,0-28,5) |
| HPV45 | 0/871 | 4652,5 | 0,0
(0,0-7,9) |
0/261 | 1298,6 | 0,0
(0,0-28,4) |
| HPV52 | 0/870 | 4645,5 | 0,0
(0,0-7,9) |
2/261 | 1294,2 | 15,5
(1,9-55,8) |
| HPV58 | 0/863 | 4613,5 | 0,0
(0,0-8,0) |
0/259 | 1293,2 | 0,0
(0,0-28,5) |
| Bệnh tật liên quan đến HPV6/11/16/18/31/33/
45/52/58 |
1/866 | 4576,1 | 2,2
(0,1-12,2) |
0/261 | 1278,6 | 0,0
(0,0-28,9) |
| Ung thư cổ tử cung mức độ 1 | 1/866e | 4573,9 | 2,2
(0,1-12,2) |
— | — | — |
| Ung thư cổ tử cung mức độ 2 hoặc 3 | 0/866 | 4577,5 | 0,0
(0,0-8,1) |
— | — | — |
| Ung thư biểu mô tại chỗ | 0/866 | 4577,5 | 0,0
(0,0-8,1) |
— | — | — |
| Ung thư cổ tử cung | 0/866 | 4577,5 | 0,0
(0,0-8,1) |
— | — | — |
| Sùi mào gà | 0/866 | 4579,6 | 0,0
(0,0-8,1) |
0/261 | 1278,6 | 0,0
(0,0-28,9) |
| Ung thư âm hộ mức độ 1 hoặc tình trạng tệ hơn | 0/866 | 4579,6 | 0,0
(0,0-8,1) |
— | — | — |
| Ung thư âm đạo hoặc tình trạng tệ hơn | 0/866 | 4579,6 | 0,0
(0,0-8,1) |
— | — | — |
| Tân sinh biểu mô dương vật mức độ 1 hoặc tình trạng tệ hơn | — | — | — | 0/261 | 1278,6 | 0,0
(0,0-28,9) |
Độ an toàn của vắc xin
Không có báo cáo nào về biến cố bất lợi liên quan đến vắc xin trong thời gian theo dõi 10 năm. Một người tham gia trong nghiên cứu tử vong sau 8,6 năm dùng liều vắc xin thứ 3 do bệnh lao (không liên quan đến vắc xin 9vHPV sử dụng).
Kết luận
Vắc xin 9vHPV đã chứng minh được khả năng sinh miễn dịch và hiệu quả bền vững cũng như độ an toàn trong 10 năm cho trẻ nam và trẻ nữ từ 9 đến 15 tuổi.
Nguồn: Restrepo J, Herrera T, Samakoses R, et al., Pediatrics. 2023;152(4):e2022060993
Biên tập: ThS.DS Nguyễn Nguyệt Minh, DS. Lê Thị Nguyệt Minh