1. Bối cảnh và mục tiêu nghiên cứu
Hội chứng thận hư (HCTH) tiên phát là bệnh cầu thận mạn tính phổ biến ở trẻ em. Dù 80-90% đáp ứng với steroid, nhưng khoảng 50-60% sẽ phát triển thành HCTH tái phát thường xuyên (Frequently Relapsing Nephrotic Syndrome – FRNS) hoặc phụ thuộc steroid (Steroid Dependent Nephrotic Syndrome – SDNS). Các phương pháp điều trị chuẩn cho FRNS/SDNS, như dùng steroid kéo dài hoặc các thuốc ức chế miễn dịch (ƯCMD) khác như cyclosporine, mycophenolate mofetil, cyclophosphamide, thường đi kèm lo ngại về độc tính của thuốc, nguy cơ vô sinh, hoặc tỷ lệ tái phát cao sau khi ngừng thuốc.
Rituximab, một kháng thể đơn dòng kháng CD20, đã được chứng minh là có hiệu quả đối với HCTH biến chứng (những bệnh nhân đã tái phát hoặc phụ thuộc steroid trong hoặc sau khi điều trị bằng các thuốc ƯCMD khác). Tuy nhiên, chưa có thử nghiệm lâm sàng ngẫu nhiên, có đối chứng đánh giá hiệu quả của rituximab trên bệnh nhân mắc HCTH không biến chứng (FRNS/SDNS chưa được điều trị bằng thuốc ƯCMD khác ngoài glucocorticoid). Do đó, mục tiêu chính của nghiên cứu này là đánh giá hiệu quả và an toàn của rituximab trong điều trị HCTH không biến chứng ở trẻ em trong vòng một năm thông qua thử nghiệm lâm sàng ngẫu nhiên, mù đôi, có đối chứng giả dược được thực hiện đa trung tâm.
2. Phương pháp nghiên cứu
2.1. Thiết kế:
Thử nghiệm lâm sàng đa trung tâm, mù đôi, ngẫu nhiên, có đối chứng giả dược, nhóm song song.
Các bệnh nhân với HCTH tái phát được lựa chọn và sau khi đạt được lui bệnh hoàn toàn với phác đồ prednisolone tiêu chuẩn được tiến hành phân ngẫu nhiên. Nhóm rituximab nhận một liều 375 mg/m2 (tối đa 500 mg) truyền tĩnh mạch hàng tuần trong 2 tuần. Nhóm đối chứng nhận giả dược tương ứng. Thử nghiệm được theo dõi trong 1 năm, và sau đó một nghiên cứu theo dõi được thực hiện để đánh giá tiên lượng lâu dài.
2.2. Đối tượng nghiên cứu:
– Tiêu chí lựa chọn:
- Được chẩn đoán HCTH vô căn theo tiêu chuẩn của International Study of Kidney Disease in Children.
- Bệnh khởi phát trước 18 tuổ
- Được chẩn đoán là FRNS hoặc SDNS trước ngày phân nhóm nghiên cứ
- Chưa từng điều trị bằng các thuốc ƯCMD nào khác ngoài glucocorticoid.
– Tiêu chí loại trừ:
- Được chẩn đoán HCTH kháng steroid.
- Bị HCTH thứ phát hoặc hội chứng viêm thậ
- Có tiền sử nhiễm trùng nặ
- Đã từng nhận bất kỳ loại kháng thể đơn dòng nào trước đó.
2.3. Tiêu chí đánh giá:
– Tiêu chí chính: Thời gian không tái phát (thời gian từ lúc phân nhóm ngẫu nhiên đến lần tái phát đầu tiên) trong giai đoạn mù đôi 1 năm.
– Tiêu chí phụ: Thời gian đến khi thất bại điều trị; liều corticosteroid hằng ngày; thời gian giảm tế bào B ngoại vi.
– Các biến cố bất lợi: Được ghi nhận và đánh giá theo Tiêu chí thuật ngữ chung về các biến cố bất lợi (Common Terminology Criteria for Adverse Events) trong cả hai giai đoạn làm mù và mở nhãn.
3. Kết quả
3.1 Hiệu quả (trong 1 năm theo dõi nghiên cứu)
– Tiêu chí chính:
- Thời gian không tái phát ở nhóm rituximab dài hơn so với nhóm giả dược: trung vị (KTC 95%) 285 ngày (173 – chưa đạt) so với 81 ngày (66–100); p<0.001 và HR (Hazard Ratio): 0,27 (KTC 95%: 0,12–0,59).
- Số bệnh nhân tái phát: Nhóm rituximab 10/18; nhóm giả dược 20/22.
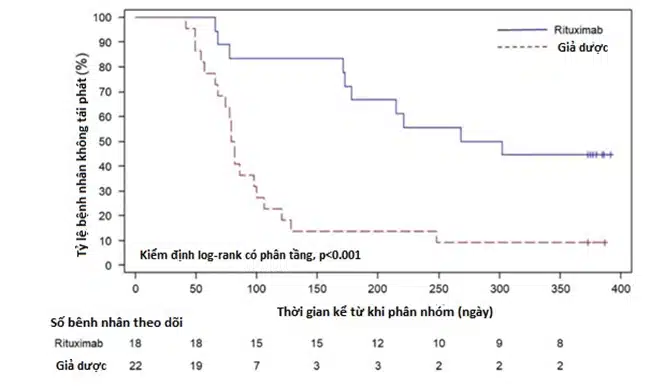
Hình 1: Biểu đồ đường Kaplan–Meier thời gian và bảng theo dõi số bệnh nhân không tái phát trong 1 năm theo dõi thử nghiệm
– Tiêu chí phụ:
- Số bệnh nhân thất bại điều trị: nhóm rituximab có 8 và nhóm giả dược có 19 bệnh nhân. Thời gian đến khi thất bại điều trị ở nhóm rituximab dài hơn so với nhóm giả dược: trung vị (KTC 95%): chưa đạt được (175 – chưa đạt) so với 84 ngày (70–102); HR = 0,24 (KTC 95%: 0,10–0,57).
- Liều corticosteroid ở nhóm rituximab là 0,36 (±0,22) mg/kg/ngày và thấp hơn so với nhóm giả dược là 0,89 (±0,37) mg/kg/ngày, p < 0,001.
- Giảm tế bào B ngoại vi (< 5 tế bào/µL): được quan sát ở 15/18 bệnh nhân trong nhóm Rituximab, và tất cả đều hồi phục ≥ 5 tế bào/µL vào ngày thứ 179
3.2 An toàn (trong 1 năm theo dõi nghiên cứu):
– Không có sự khác biệt về tổng tỷ lệ biến cố bất lợi giữa hai nhóm.
– Phản ứng liên quan đến truyền dịch xảy ra nhiều hơn đáng kể ở nhóm rituximab: 61% (KTC 95%: 36-83%) so với 9% (KTC 95%: 1-29%) ở nhóm giả dược; p<0.001. Tuy nhiên, tất cả các phản ứng này đều ở mức độ nhẹ (độ 1 hoặc 2) và tự khỏi trong vòng 24 giờ.
– Không có biến cố bất lợi nghiêm trọng nào xảy ra ở nhóm rituximab.
3.3 Nghiên cứu theo dõi (Dài hạn):
Kết quả theo dõi cho thấy sự khác biệt vẫn được duy trì. Tỷ lệ sống không tái phát tích lũy sau 3 năm (mà không cần điều trị thêm) ở nhóm Rituximab là 38% (KTC 95%: 17–60%), ở nhóm giả dược là 9% (KTC 95%: 2–25%).
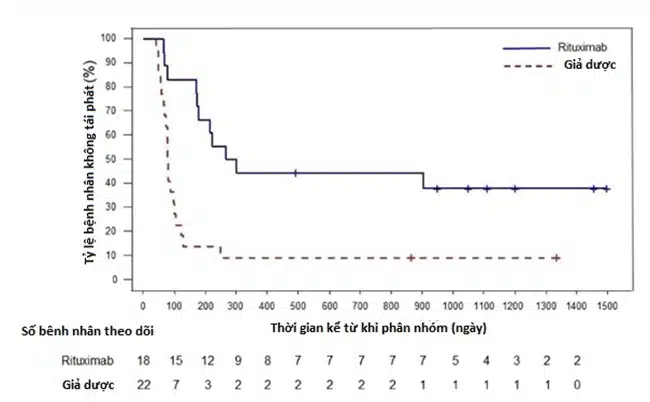
Hình 2: Biểu đồ đường Kaplan–Meier thời gian và bảng theo dõi số bệnh nhân không tái phát từ giai đoạn mù và giai đoạn theo dõi tiếp theo
4. Kết luận
Nghiên cứu chỉ ra rituximab không chỉ kéo dài đáng kể thời gian không tái phát trong 1 năm, mà còn có khả năng mang lại sự lui bệnh lâu dài. Tỷ lệ lui bệnh đến 3 năm khi dùng rituximab ở nhóm HCTH không biến chứng (38%) cũng cao hơn đáng kể so với các báo cáo trước đây về HCTH biến chứng (6% – 20%).
Sự khác biệt về hiệu quả lâu dài này có thể là do việc điều trị bằng rituximab được thực hiện sớm hơn. Trong nghiên cứu này, thời gian trung bình từ khi chẩn đoán FRNS/SDNS đến khi dùng rituximab chỉ là 29 ngày (trong giai đoạn mù đôi), so với các nghiên cứu khác (có tỷ lệ lui bệnh dài hạn thấp hơn) là khoảng 2,5 năm kể từ khi khởi phát HCTH.
Qua kết quả nghiên cứu cho thấy rituximab có thể là một lựa chọn điều trị đầu tay ở trẻ em bị FRNS/SDNS không biến chứng, đặc biệt là ở những bệnh nhân trong giai đoạn đầu của bệnh.
Tuy nhiên, nghiên cứu còn một số hạn chế bao gồm việc không so sánh rituximab trực tiếp với các thuốc ƯCMD khác, cỡ mẫu nhỏ (18 dùng rituximab và 22 dùng giả dược).
Biên tập: ThS.DS. Nguyễn Văn Dũng, DS. Nguyễn Việt Anh
Nguồn: Iijima K, Sako M, et al. Sci Rep. 2025 Oct 10;15(1):34306. Doi: 10.1038/s41598-025-19214-0.



![[Thư cảm ơn] Nhân dịp khai trương Bệnh viện Nhi Trung ương cơ sở 2](https://benhviennhitrunguong.gov.vn/wp-content/uploads/2026/06/thu-cam-on-khai-truong-cs2_540x360-150x150.png)



